2025.02.17
原代肝实质细胞(肝细胞,Hepatocytes)三明治夹层培养模型的开发是模拟体内肝脏微环境的一项重要技术。与传统2D单层培养模型相比,该模型通过将肝细胞夹置于两层细胞外基质(ECM,如I型胶原和Matrigel)之间,不仅重建了细胞极性,还显著延长了肝细胞功能的维持时间,使其成为研究胆小管网络形成、药物代谢酶活性(如CYP450家族)及多种转运蛋白功能的理想工具。
自20世纪90年代由Liu X、Lecluyse EL和Brouwer KR等人开发,三明治夹层培养模型在解决单层肝细胞快速去分化和功能 丧失的挑战中取得了显著成效。该模型能够维持肝细胞的胆汁排泄功能,并为研究药物代谢、肝毒性及转运机制提供了高效且生 理相关的体外药物研究模型。
三明治夹层培养模型以其卓越的长期功能维持能力,在多个领域展现出重要价值:
药物代谢与药代动力学(DMPK)研究
胆道清除评估
药物性肝损伤(DILI)研究
肝胆转运蛋白功能分析
跨物种肝细胞研究
妙顺生物TPCS®原代肝实质细胞三明治夹层培养系统整合了高质量的冻存肝实质细胞与优化的外基质胶(Matrigel),为构建高性能肝细胞三明治夹层培养模型提供了可靠的解决方案。
冻存肝实质细胞的多物种支持
TPCS®冻存原代肝实质细胞覆盖大鼠、小鼠、猴和犬等多个物种,细胞经过贴壁三明治夹层培养验证,保证高贴壁率与卓越的细胞质量。这些特点对构建稳定的三明治夹层培养模型及其后续应用至关重要。
夹层培养模型的表征与验证
为了验证该优化系统的性能,我们采用CDF荧光探针检测胆小管形成及MRP2介导的CDF转运功能。结果显示,三明治夹层培养模型中的肝细胞能够形成密集的胆小管网络,并观察到明显的荧光CDF在胆小管中的累积。这表明系统能够有效重建肝细胞的极性和转运功能。
药物代谢活性的增强
为评估TPCS®三明治夹层培养系统的药物代谢活性,我们使用特异性底物探针测定I相和II相代谢酶活性。结果显示,与传统2D单层培养相比,三明治夹层培养显著提高了多种代谢酶的活性,进一步凸显其在药物代谢和毒性研究中的应用潜力。
[示例]:冻存SD大鼠原代肝实质细胞三明治夹层培养
材料与方法
原代肝实质细胞 : 冻存SD大鼠原代肝实质细胞(TPCS®,货号CRH-100SDP-PQ, 经贴壁和夹层培养验证批次)。
包被培养基 : HCM-R,包括两种组分和两种规格:
基础培养基 (HCM-BM-40, 40 mL) 和鼠尾胶原蛋白I型(AR0001-02,1 mg),
基础培养基 (HCM-BM-120, 120 mL)和鼠尾胶原蛋白I型(AR0001-05,2.5 mg)。
Matrigel基质胶。
肝细胞复苏优化培养基 : 即用型完全培养基(TPCS®,货号HTS-R-120WP/HTS-R-40WP)。
肝细胞铺板培养基 : 即用型完全培养基(TPCS®,货号HPM-R-40/120)。
肝细胞维持培养基 : 即用型完全培养基(TPCS®,货号HMM-R-120P/HMM-R-40)。
CDFDA(5-氯甲基荧光素二乙酸酯)。
0.4%台盼蓝。
夹层培养操作分为以下6个主要步骤 (见如下示意图)
肝细胞“三明治”夹层培养流程示意图
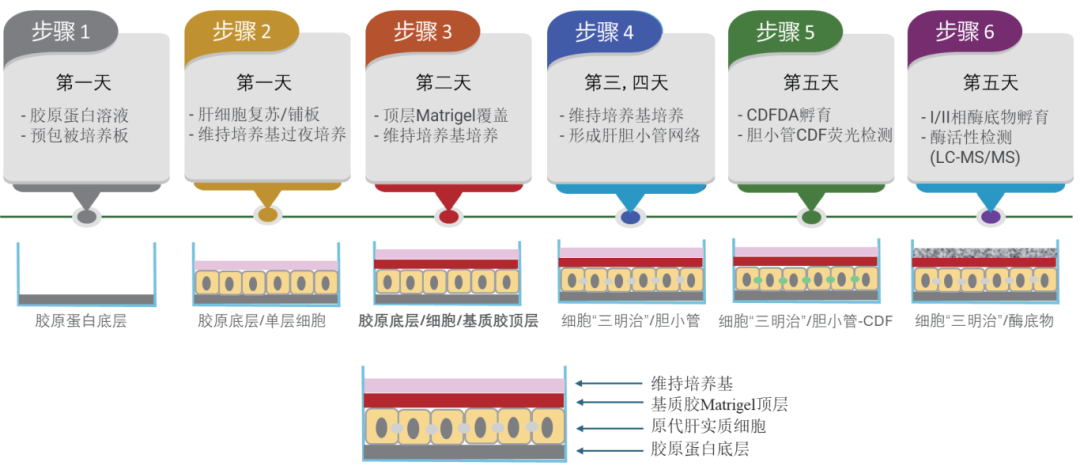
图 1 : 肝细胞“三明治”夹层培养流程示意图
肝细胞“三明治”架构
1:三明治夹层培养肝细胞中胆小管的形成及荧光CDF的累积
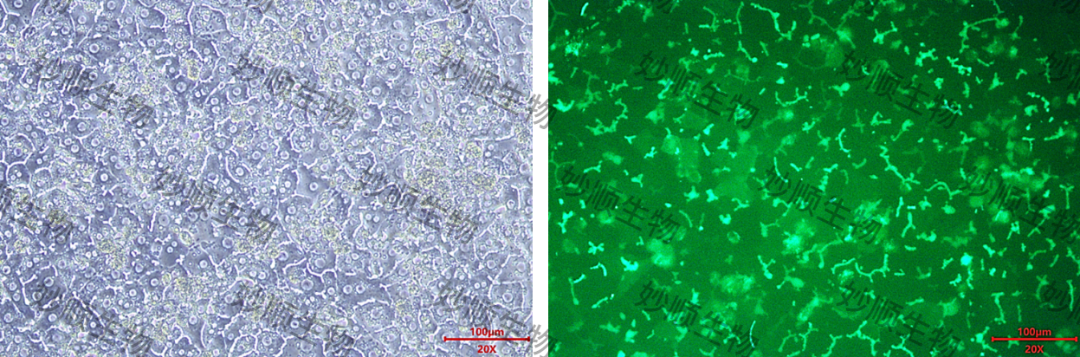
图 2:SD大鼠肝细胞胆小管的荧光CDF累积结果。将SD大鼠肝细胞按照指定密度接种至胶原蛋白预包被的24孔细胞培养板中,在三明治夹层培养条件下,SD大鼠肝细胞于培养第3-4天形成了清晰且密集的胆小管网络(左图)。在用CDFDA孵育10-15分钟后, 观察到由MRP2介导的CDF荧光在胆小管网络中显著分布和累积(右图)。
2:肝细胞三明治夹层培养模型与传统2D单层培养酶活性比较
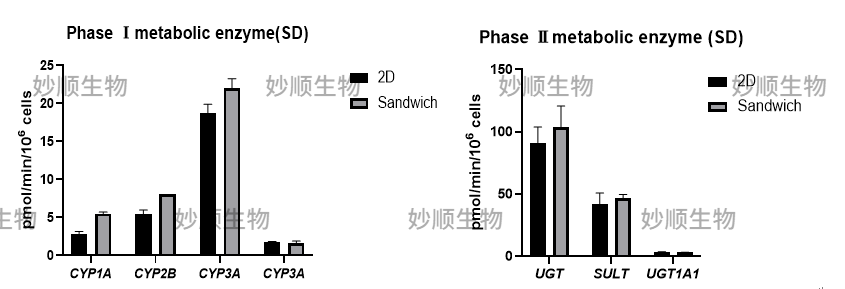
图 3 : 在37°C条件下,以指定底物浓度分别孵育三明治夹层培养和传统2D单层培养的肝细胞60分钟后,通过LC-MS/MS技术检测生成的代谢产物。I相和II相酶的代谢活性以代谢产物的形成速率计算,结果以每百万细胞每分钟生成的代谢产物皮摩尔数( pmol/min/106 cells)表示,用于表征相应酶的活性。
使用TPCS®原代肝实质细胞成功构建了SD大鼠肝细胞三明治模型。通过CDFDA荧光染色实验结果,显示该模型形成了完整的胆小管结构,并保持了优良的胆小管功能。与2D单层培养相比,三明治夹层培养模型能够更好地维持肝细胞的代谢功能和整体活性, 使其在药物筛选、毒理学研究和药物代谢研究中具有显著优势。
如有需要请联系我们


妙顺生物
咨询热线:021-64169739
咨询邮箱:sales@miles-bio.com